哺乳动物细胞培养过程中的糖摄取
在细胞培养过程中,细胞无时无刻不在进行分解代谢,从而为其各项生命活动提供源源不断的能量。糖类是细胞中重要的能源物质,且只有单糖才能进入分解代谢途径,所以多糖首先需要通过细胞的酶促降解变为单糖才能被细胞利用。自然界存在各种各样的单糖(如葡萄糖、果糖、半乳糖、甘露糖等),但不管是高等的多细胞真核生物还是低等的单细胞原核生物,均优先利用葡萄糖(glucose)。基于此特征,在哺乳动物细胞培养过程中一般优先使用葡萄糖作为主要碳源。
在哺乳动物细胞内,细胞主要通过摄取葡萄糖为其生命活动提供能量,进入膜内的葡萄糖在己糖激酶的催化下生成6-磷酸葡萄糖,通过糖酵解生成丙酮酸,在线粒体内丙酮酸进入三羧酸循环被氧化生成CO2。
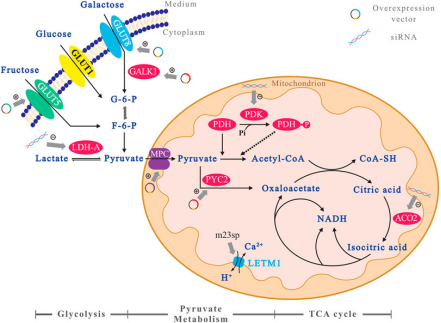
图1 细胞内糖的代谢过程
由于葡萄糖具有亲水性,不能通过简单的膜扩散作用通过质膜,因此需要通过特定的转运体才能进入细胞。葡萄糖转运体(glucose transporter)主要有两个家族,根据其功能和结构特性分为促进葡萄糖转运蛋白家族(GLUTs)和钠-葡萄糖共转运蛋白家族(SGLTs)。
GLUT家族
GLUTs以易化扩散的方式顺浓度梯度转运葡萄糖,其转运过程不消耗ATP。目前,该家族有14个不同的成员,根据其序列同源性分为3类。
I类包括GLUT1、GLUT2、GLUT3、GLUT4和GLUT14;
II类包括果糖转运体GLUT5、GLUT7、GLUT9和GLUT11;
III类包括GLUT6、GLUT8、GLUT10、GLUT12和GLUT13(HMIT)。
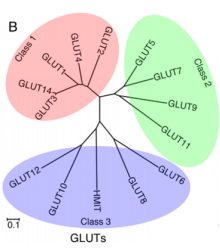
图2 依据蛋白序列的相似性GLUTs分组情况
其中,GLUT1在哺乳动物细胞中分布最广泛,其结构如图3所示。
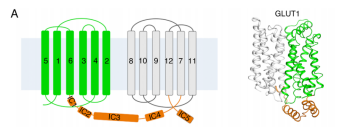
图3 GLUT1结构 12个跨膜螺旋被分为N域和C域,分别为绿色和白色。细胞内螺旋结构域(ICH)呈橙色
GLUT1在哺乳动物细胞的葡萄糖摄取中起到了重要作用。哺乳动物细胞摄取葡萄糖受生长因子调节,生长因子可通过调节PI3K/AKT通路诱导GLUT1从细胞囊泡运输到质膜,促进葡萄糖摄取。
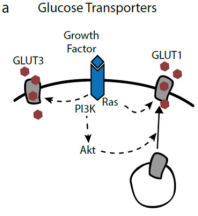
图4 PI3K/AKT通路信号调节哺乳动物细胞中营养摄取通路
除PI3K/AKT通路外,GLUT1对葡萄糖摄取还受AMPK通路调节。当哺乳动物细胞处于代谢压力的情况下,如:低氧分压、氧化磷酸化阻断、渗透压改变,AMPK通过抑制硫氧还蛋白互作蛋白(TXNIP)介导的内吞作用来增加质膜中GLUT1的浓度,通过磷酸化GLUT1直接增加其葡萄糖转运速率。使得细胞从糖酵解中获得更多的ATP,以供代谢之需。
GLUTs还存在多个胰岛素依赖型家族成员(GLUT4,GLUT8,GLUT12等)。例如,GLUT4主要在胰岛素刺激后发挥作用。在静息状态下,GLUT4存储于GLUT4存储囊泡(GSVs)中,当有胰岛素刺激后,GLUT4从GSVs易位到质膜,在质膜中促进葡萄糖转运至胞内。
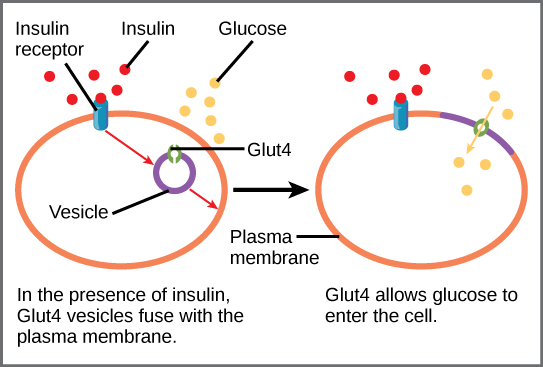
图5 胰岛素调节GLUT4的细胞内转运
SGLT家族
SGLTs是钠依赖性葡萄糖转运体,以主动转运方式转运葡萄糖。其并不能直接利用ATP,需要利用由Na+/K(+)-ATPase维持的钠离子梯度,驱动葡萄糖进入细胞。SGLT家族主要有六位成员。
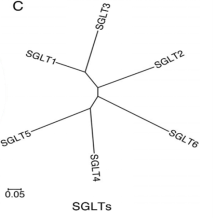
图6 SGLT分类
SGLTs中以SGLT1以及SGLT2研究较多。SGLT1对Na+和葡萄糖以2:1的比例同时进行转运,SGLT2
对Na+和葡萄糖以
1:1 的比例同时进行转运。
虽然葡萄糖可通过葡萄糖转运体转运至细胞内作为哺乳动物细胞培养中的主要糖源,但葡萄糖的消耗通常导致丙酮酸积累和乳酸浓度增加,高浓度乳酸会抑制哺乳动物细胞培养过程中的细胞生长。因此,各研究团队也在积极寻找哺乳动物细胞培养过程中的其他可利用糖源。
C.Altamirano等人使用果糖、半乳糖和甘露糖分别作为糖源进行批式实验,结果表明使用半乳糖或果糖这类代谢较慢的糖作为糖源可减少细胞内乳酸的积累。然而,由于半乳糖、果糖做糖源时摄取效率远低于葡萄糖,因此会对细胞生长密度造成显著影响,进而影响抗体浓度。
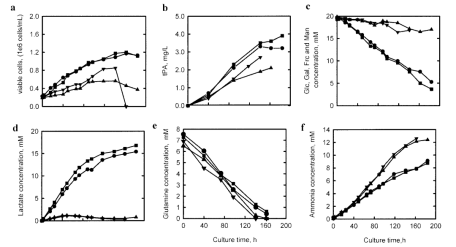
图8 使用四种不同的糖源的批式培养结果:20mM果糖(▲)、20 mM半乳糖(▼)、20 mM甘露糖(■)和20 mM葡萄糖(●)(对照)
除单糖外,研究人员也在考虑寡糖(Oligosaccharide)作为替代糖源的可行性。Dawn Sow Zong Leong等人将不同哺乳动物细胞在不同糖源的培养基中进行培养,结果表明,除葡萄糖培养基外,麦芽糖培养基中细胞的活力和活细胞密度在第14天开始上升。表明哺乳动物细胞可以在利用麦芽糖为糖源的培养基中增殖。
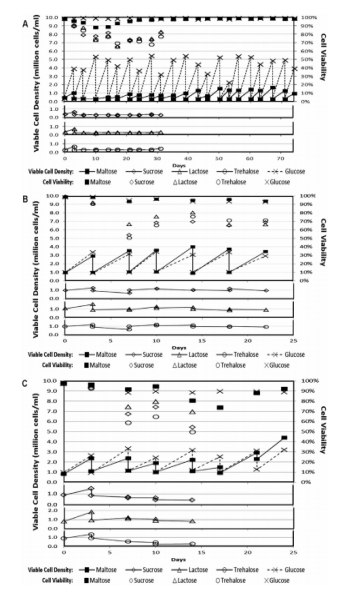
图10
细胞在各种双糖培养基中的适应性
(A) CHO-K1 (B) CHO-DG44 (C) HEK293[8]
为了进一步评估麦芽糖对于哺乳动物细胞生长的情况,研究者将细胞在含有不同浓度麦芽糖培养基中培养。结果表明,随着麦芽糖浓度升高,细胞增殖速率更快。
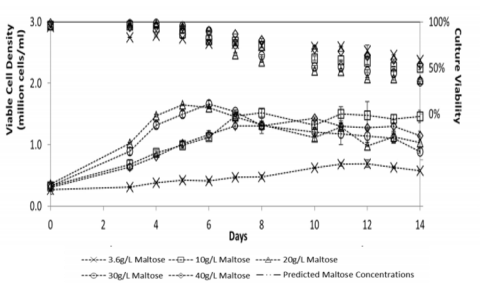
图11
细胞在不同浓度麦芽糖培养基中的生长情况[9]
相较于14 g/L葡萄糖培养基中培养的细胞,使用麦芽糖作为糖源的细胞在第8天后活细胞密度下降较快,10 g/L麦芽糖培养基中细胞活率下降较快。然而,目前对使用麦芽糖作为糖源的研究仍较少,具体应用仍需进一步研究。
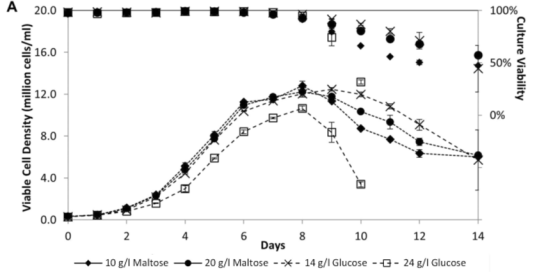
图12 细胞在不同培养基中生长情况
虽然目前对哺乳动物细胞葡萄糖转运机制尚未完全明确,替代葡萄糖的其他可利用糖源也在探索中,但现有研究结果表明,哺乳动物细胞可在麦芽糖、半乳糖作为糖源的培养基中增殖,但其具体的作用机制仍需进一步研究。可以预见,对哺乳动物细胞中葡萄糖的转运机制的研究会更深入,替代糖源的利用方式会被进一步挖掘。
参考文献
[1]Huan-Yu Zhang, Zhen-Lin Fan, Tian-Yun Wang. Advances of Glycometabolism Engineering in Chinese Hamster Ovary Cells [J]. Front Bioeng Biotechnol. 2021 Dec 2;9:774175. doi: 10.3389/fbioe.2021.774175. eCollection 2021.
[2]Deng D, Yan. GLUT, SGLT, and SWEET: Structural and mechanistic investigations of the glucose transporters[J]. Protein Sci, 2016, 25: 546-58. DOI:10.1002/pro.2858
[3]Palm, W., Thompson, C. Nutrient acquisition strategies of mammalian cells. Nature 546, 234–242 (2017). DOI:10.1038/nature22379
[4]Glucose Transporters GLUT and SGLT: Biochemistry, MCAT, and USMLE – Moosmosis, https://moosmosis.org/2020/07/21/glucose-transporters-glut-and-sglt-biochemistry/
[5]Madunić I V, Madunić J, Breljak D, et al. Sodium-glucose cotransporters: new targets of cancer therapy?[J]. Arh Hig Rada Toksikol, 2018, 69: 278-285. DOI:10.2478/aiht-2018-69-3204
[6]Altamirano C, Paredes C, Cairó J J, et al. Improvement of CHO cell culture medium formulation: simultaneous substitution of glucose and glutamine[J]. Biotechnol Prog, 2000, 16: 69-75. DOI: 10.1021/bp990124j
[7]Jiménez N, Martínez V S, Gerdtzen Z P. Engineering CHO cells galactose metabolism to reduce lactate synthesis[J]. Biotechnol Lett, 2019, 41: 779-788. DOI:10.1007/s10529-019-02680-8
[8]Leong D S Z, Tan J G L, Chin C L, et al. Evaluation and use of disaccharides as energy source in protein-free mammalian cell cultures[J]. Sci Rep, 2017, 7: 45216. DOI:10.1038/srep45216
[9]Leong D S Z ,Teo B K H, Tan J G L, et al. Application of maltose as energy source in protein-free CHO-K1 culture to improve the production of recombinant monoclonal antibody[J]. Sci Rep, 2018, 8: 4037. DOI: 10.1038/s41598-018-22490-8

 微信公众号
微信公众号